Преимплантационная генетическая диагностика эмбриона является частью процедуры экстракорпорального оплодотворения. В неё входит биопсия эмбриона, использование флуоресцентной гибридизации in situ, либо полимеразной цепной реакции на уровне отдельных клеток. Это сложная процедура, требующая большого опыта врача-генетика. В этой статье мы расскажем, что входит в преимплантационную генетическую диагностику, как она проводится, и какие возможности открывает ПГД (ПГТ) в нашем центре.
Что такое ПГД?
Определение
Преимплантационная генетическая диагностика (ПГД) обычно определяется как тестирование эмбрионов или ооцитов на преимплантационной стадии для того, чтобы проверить наличие или подтвердить отсутствие у них генетических дефектов. Этот тип диагностики был разработан для семейных пар, чьи потенциальные дети подвержены риску тяжелых менделевских нарушений, структурных хромосомных аномалий или митохондриальных нарушений.
Основное преимущество использования ПГД для скрининга определенного генетического заболевания заключается в том, что оно позволяет избежать селективного аборта, поскольку этот метод повышает вероятность того, что ребенок не будет иметь рассматриваемого заболевания. ПГД является дополнением к вспомогательным репродуктивным технологиям и требуют экстракорпорального оплодотворения (ЭКО) для получения материала для анализа – обычно это биопсия трофэктодермы (оболочки эмбриона), которая происходит на стадии бластоцисты.
Источник: Progen
Как правильно: ПГТ или ПГД?
Преимплантационная генетическая диагностика (ПГД) и преимплантационное генетическое тестирование (ПГТ) — это синонимы одного и того же направления генетической диагностики. Раньше под ПГД понимали исследование эмбриона только на моногенные заболевания или структурные хромосомные перестройки, а для исследования на анеуплоидии применяли понятие преимплантационный генетический скрининг. Сейчас оба термина, преимплантационный скрининг и преимплантационная генетическая диагностика, объединены понятием преиплантационного генетического тестирования (ПГТ).
Преимплантационная генетическая диагностика эмбрионов, какие виды ПГД существуют?
В настоящее время существует три различных типа ПГД: преимплантационное генетическое тестирование анеуплодий (ПГТ-А), преимплантационное генетическое тестирование моногенных заболеваний (ПГТ-М) и преимплантационное генетическое тестирование стуктурных перестроек (ПГТ-СП). Для проведения ПГТ-М и ПГТ-СП семья должна быть информативна по конкретной генной мутации или хромосомной перестройке (диагноз должен быть установлен и подтвержден генетическими методами).
ПГТ-А — это полногеномное исследование биоптата трофэктодермы эмбриона, которое с высокой точностью выявляет численные и структурные хромосомные нарушения, называемые анеуплоидиями.
ПГТ-М — это генетическое исследование биоптата трофэктодермы эмбриона на наличие определенной генетической мутации (патогенного варианта) или нескольких вариантов, ассоциированных с наследственным заболеванием.
ПГТ-СП — это генетическое исследование биоптата трофэктодермы эмбриона на наличие структурных хромосомных нарушений.
Поскольку большинство ранних потерь беременности можно отнести к анеуплоидии, ПГТ-А является важнейшим преимплантационным диагностическим тестом. ПГТ-А позволяет лучше выбирать эмбрионы, что повышает частоту имплантации при переносе одного эмбриона и снижает частоту выкидышей. Поскольку в матку переносят только эмбрионы с нормально сформированным хромосомным набором, риск потери плода в первом и втором триместрах значительно снижается.
В чём преимущество ПГТ?
Поскольку в матку для имплантации переносят только эмбрионы без генетических нарушений, ПГТ является единственным доступным методом скрининга эмбрионов до беременности и, для семей высокого генетического риска, представляет собой альтернативу современным диагностическим процедурам после зачатия естественным путем (например, амниоцентезу или биопсии ворсин хориона), за которыми часто может последовать необходимость принятия семьей трудного решения о прерывании беременности.
ПГТ в настоящее время является единственным доступным вариантом, позволяющим избежать высокого риска рождения ребенка с генетическим заболеванием до имплантации. Это привлекательное средство предотвращения наследственных генетических заболеваний, тем самым устраняя дилемму прерывания беременности после неблагоприятного пренатального диагноза.
В возрастной группе женщин старше 35 –37 лет проведение ПГТ-А улучшило показатель живорождения и снизило частоту выкидышей с 39% до 2,7%. Оно также продемонстрировало более короткое время до наступления беременности.
Достижения в области культивирования эмбрионов, методов биопсии бластоцисты, платформ для скрининга 24-хромосомной анеуплоидии и улучшенного геномного охвата новых платформ секвенирования, таких как секвенирование следующего поколения (NGS), сделали ПГТ безопасным и доступным для всех пациентов, подвергающихся экстракорпоральному оплодотворению. Современный подход к ЭКО включает культуру бластоцисты и биопсию с последующей ПГТ и переносом одного эмбриона.
Кому показано проведение ПГД?
- Женщинам возрастной группы риска из-за повышения вероятности аномальной генетики эмбриона при нормальном репродуктивном старении. В возрастной группе женщин старше 35 –37 лет проведение ПГТ-А улучшило показатель живорождения и снизило частоту выкидышей с 39% до 2,7%. Оно также продемонстрировало более короткое время до наступления беременности.
- Пары, у которых есть риск рождения ребенка с наследственным генетическим заболеванием
- История повторных выкидышей из-за хромосомных аномалий
- Парам с повторными неудачами ЭКО
- Пары, отягощенные тяжелым мужским фактором бесплодия
Эти группы пациентов подвержены риску неудачи ЭКО из-за высокой доли анеуплоидных эмбрионов. Считается, что ПГТ-А снижает этот риск за счет выбора эмбрионов с нормально сформированным хромосомным набором с более высокой вероятностью имплантации.
Парам, у которых есть высокий риск рождения ребенка с наследственным генетическим заболеванием, ПГТ-М помогает выбрать эмбрионы с благоприятным прогнозом по этому заболеванию или предотвратить передачу семейной мутации дальнейшим поколениям.
Как проводится анализ ПГД?
Прежде чем проводить предимплантационное генетическое тестирование, кандидаты должны проконсультироваться с врачом-генетиком, чтобы оценить риск передачи их генетической аномалии их потомству. Должны быть выполнены тесты для подтверждения диагноза больного родителя, для точного определения генетического изменения, приводящего к рассматриваемому состоянию, и для гарантии того, что доступная в настоящее время технология может идентифицировать это генетическое изменение.
Работаете в клинике ЭКО?
Обратитесь к нашему менеджеру, чтобы узнать о возможностях сотрудничества с PROGEN в проведении ПГД для своих пациентов. Мы занимаемся преимплантационной генетической диагностикой уже более 8 лет. Мы постоянно работаем над новыми инновационными решениями, чтобы люди получили достойный результат, а не красивый бланк.
Чтобы получить эмбрионы для биопсии для ПГТ, пациенты должны пройти экстракорпоральное оплодотворение (ЭКО). После оплодотворения яйцеклетки сперматозоидами эмбрионам дают возможность развиться в бластомеры 5-го дня. На 5 сутки проводят биопсию нескольких клеток трофэктодермы эмбриона. В большинстве случаев после выполнения биопсии эмбрионы замораживают и переносят позже, учитывая сроки завершения ПГТ.
Генетическая диагностика ПГТ в настоящее время выполняется с использованием секвенирования следующего поколения (NGS), иногда в сочетании с ПЦР. Ранее для генетического анализа эмбриона использовали методы FISH (флюоресцентная гибридизация in situ) и сравнительной геномной гибридизации (CGH). Непораженные и/или эуплоидные эмбрионы затем переносят в матку для последующей имплантации.
Экстракорпоральное оплодотворение (ЭКО)
Процедура ЭКО состоит из стимуляции яичников, извлечения яйцеклетки, оплодотворения яйцеклетки, развития эмбриона и переноса эмбриона (см. изображение ниже).
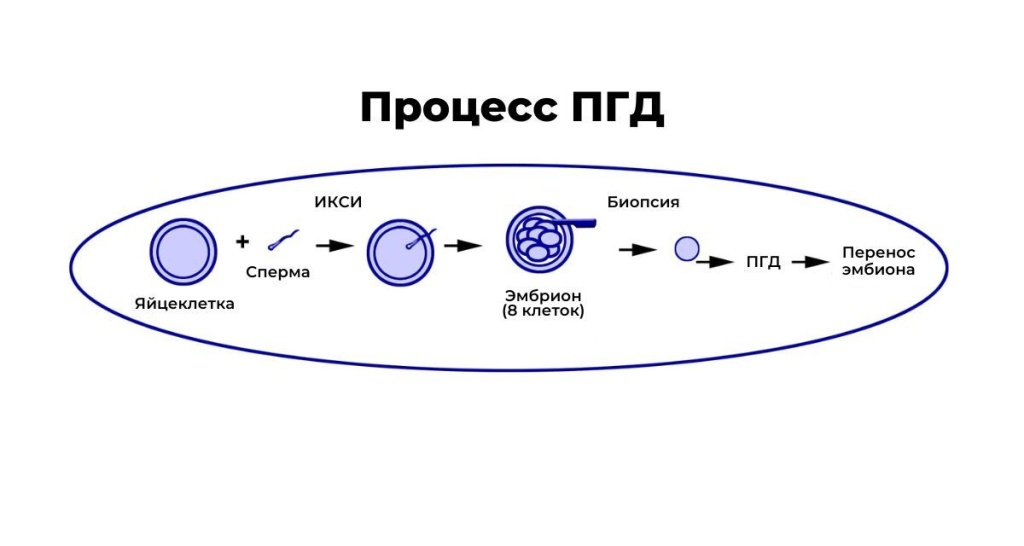
Шаги можно обобщить следующим образом:
Стимуляция яичников, необходимая для производства нескольких яйцеклеток. В течение 8–14-дневного периода гормональной стимуляции проводятся частые ультразвуковые исследования и лабораторные анализы для наблюдения за развитием и созреванием фолликулов.
Процедура забора ооцитов обычно проводится под наркозом. Под сонографическим контролем и трансвагинальным доступом фолликулы пунктируют и аспирируют их фолликулярную жидкость. Затем эмбриологи идентифицируют ооциты в эмбриологической лаборатории. Процедура обычно длится не более 15 минут.
Затем яйца культивируют в течение нескольких часов после их извлечения, чтобы обеспечить окончательное созревание. При желании, хотя сейчас это делается редко, полярное тело может быть удалено для ПГТ. Для процедуры ПГТ на более поздних стадиях эмбрионального развития предпочтительнее интрацитоплазматическая инъекция сперматозоидов (ИКСИ), при которой один сперматозоид вводится в одну яйцеклетку. Таким образом, ИКСИ предотвращает вероятность полиспермии и случайного приобретения «лишнего» хромосомного материала из сперматозоидов, что затем может повлиять на результаты ПГТ (т. е. дать ложноположительные результаты).
Сперму для оплодотворения яйцеклетки обычно получают от партнера-мужчины путем мастурбации в день извлечения яйцеклетки.
На следующее утро после ИКСИ яйцеклетки исследуют на наличие признаков оплодотворения, которые определяют по наличию 2 пронуклеусов, представляющих мужской и женский вклад в эмбрион.
Эмбрионы продолжают делиться на многоклеточные образования. Через пять дней после извлечения яйцеклеток, когда эмбрион обычно находится на стадии бластоцисты, эмбрионы можно подготовить к биопсии трофэктодермы.
Методы биопсии
В большинстве клиник выполняют биопсию трофэктодермы. Однако для ПГТ можно использовать один из трех методов: биопсия полярного тельца, биопсия эмбриона на стадии дробления или биопсия бластоцисты.
Биопсия полярного тельца
Биопсия полярного тельца работает только при женских хромосомных заболеваниях. Зрелое яйцо метафазы II выдавливает одно полярное тельце. Это полярное тельце можно удалить и протестировать, предоставив информацию только о хромосомном составе яйцеклетки. Важно отметить, что это не дает никакой информации о хромосомной конституции последующего эмбриона.
Поскольку путем анализа полярных телец можно получить информацию только о матери, хромосомные аномалии, возникающие после оплодотворения (когда сперматозоид встречается с яйцеклеткой), не обнаруживаются. Из-за этого биопсия полярного тельца используется редко.
Биопсия эмбриона на стадии дробления
Другой подход для ПГТ заключается в биопсии одного бластомера эмбрионов на 3-й день; это позволяет извлекать один бластомер из развивающегося эмбриона. Удаление бластомера является технически сложной операцией. Цель эмбриолога, достигаемая с помощью специального микроскопа и микроманипуляторов, состоит в том, чтобы удалить неповрежденную клетку с минимальным травмированием оставшегося эмбриона (см. изображение ниже).
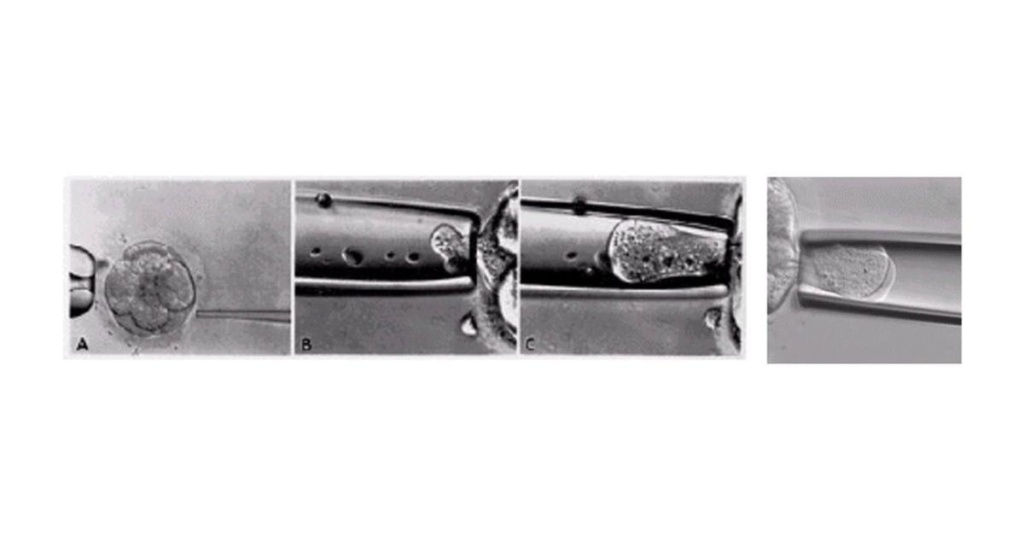
Удаление бластомера из 8-клеточного эмбриона
Перед извлечением одной клетки из 6-10-клеточного эмбриона эмбрион инкубируют в среде, не содержащей кальция и магния, в течение примерно 20 минут, чтобы уменьшить прилипание бластомеров друг к другу.
Затем эмбрион закрепляют с одной стороны удерживающей пипеткой; одновременно делается небольшое отверстие в прозрачной зоне для легкого доступа к бластомерам. Эта процедура открытия называется вспомогательным хетчингом. Вспомогательный хэтчинг может быть выполнен либо с помощью разбавленного кислого раствора Tyrode, либо с помощью лазера, либо с помощью острой кюретки. После того, как сделано маленькое отверстие, пипетка помещается через отверстие и фокусируется на выбранном бластомере, содержащем видимое ядро. Затем бластомер осторожно всасывается в пипетку и выбрасывается в окружающую среду.
Эмбрион, содержащий теперь на один бластомер меньше, возвращают в инкубатор в соответствующую культуральную среду. Затем бластомер обрабатывают, как описано ниже.
Ограничением биопсии на стадии дробления является то, что приобретенный бластомер не может быть полностью репрезентативным для всего эмбриона, поскольку эмбрионы могут быть мозаичными (т.е. эмбрионы могут состоять из более чем одной популяции клеток).
Биопсия бластоцисты
Биопсия бластоцисты на 5 день.
Эта методика стала самой популярной для ПГТ. Формирование бластоцисты начинается на 5-й день после извлечения яйцеклетки и определяется наличием внутренней клеточной массы и внешней клеточной массы или трофэктодермы. На этой стадии развития зародыш формируется из более чем 100 клеток. В прозрачной оболочке прокалывают отверстие аналогично тому, как описано для биопсии эмбриона на стадии дробления, и клетки удаляют из трофэктодермы с помощью тонкой пипетки для биопсии. Внутренняя клеточная масса остается нетронутой. Генетический анализ проводят с помощью FISH, ПЦР-анализа, CGH или NGS.
Ограничением этой процедуры является потенциальное получение клеток из трофэктодермы, которые не являются репрезентативными для развивающегося эмбриона (внутренняя клеточная масса) из-за мозаицизма (наличие нескольких различных типов клеточных линий). Кроме того, генетическое тестирование/тестирование на анеуплоидию завершается примерно через 24–48 часов после биопсии эмбриона; из-за ограниченной жизнеспособности эмбрионов в лаборатории (≤6 дней после забора яйцеклеток) биопсийные бластоцисты необходимо замораживать.
Методы оценки
Полимеразная цепная реакция
Описание
ПЦР используется для диагностики моногенных дефектов, включая доминантные и рецессивные нарушения. ПЦР, иногда называемая амплификацией ДНК, представляет собой метод, при котором конкретная последовательность ДНК многократно копируется для облегчения ее анализа. ПЦР быстро умножает одну молекулу ДНК на миллиарды молекул.
ДНК погружают в раствор, содержащий фермент ДНК-полимеразы, неприсоединенные нуклеотидные основания и праймеры. Раствор нагревают, чтобы разорвать связи между нитями ДНК. Когда раствор охлаждается, праймеры связываются с разделенными цепями, и ДНК-полимераза быстро строит новые цепи, присоединяя к праймерам свободные нуклеотидные основания. При повторении этого процесса цепь, которая была образована одним праймером, связывается с другим праймером, в результате чего получается новая цепь, специфичная исключительно к желаемому сегменту. Дальнейшие повторения процесса могут произвести миллиарды копий небольшого фрагмента ДНК за несколько часов.
Источник: Progen
ПЦР — относительно быстрый и удобный способ тестирования ДНК. Этот метод использовался в различных протоколах преимплантационного генетического тестирования. Однако для этого требуется достаточное количество чистого высококачественного образца ДНК, который иногда трудно получить из одной клетки, такой как полярное тельце или бластомер. Кроме того, возможными осложнениями являются лабораторная контаминация и выпадение аллелей.
Для ПЦР должна быть амплифицирована только одна клетка. Однако, если в пробирку попадает другая клетка или фрагмент ДНК, он также амплифицируется. Чтобы свести к минимуму эту проблему и убедиться, что нет избыточных сперматозоидов (отцовское загрязнение) и что все клетки кумулюса удалены (материнское загрязнение), необходимо использовать ИКСИ.
Лабораторная среда должна строго контролироваться, чтобы избежать попадания загрязняющих веществ в тестируемый материал. Лаборанты должны быть очень хорошо обучены, чтобы избежать любого внешнего вмешательства.
Флуоресцентная гибридизация in situ (FISH)
Описание
FISH используется для определения пола при Х-сцепленных заболеваниях, хромосомных аномалиях и скрининге анеуплоидии. FISH чаще используется при вторичном ПГД из-за его точности в скрининге анеуплоидии. Зонды (т. е. небольшие фрагменты ДНК, совпадающие с анализируемыми хромосомами) связываются с конкретной хромосомой. Каждый зонд помечен различным флуоресцентным красителем. Эти флуоресцентные зонды применяются к образцу клеточной биопсии и прикрепляются к определенным хромосомам. Их можно визуализировать под флуоресцентным микроскопом. Далее подсчитывается количество хромосом каждого типа (цвета), присутствующих в этой клетке. Таким образом, генетик может отличить нормальные клетки от аномальных клеток, таких как клетки с анеуплоидией. Хромосомы, которые можно анализировать с помощью зондов FISH, включают X, Y, 1, 13, 16, 18 и 21.
Источник: Progen
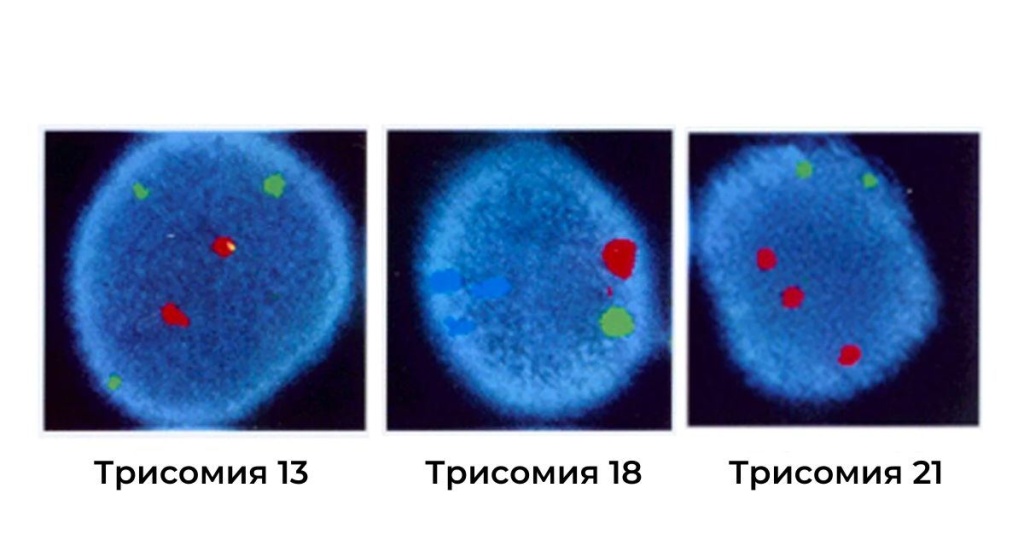
Аномалии хромосом 13, 18 и 21.
Хотя и ПЦР, и FISH широко использовались на ранних стадиях ПГТ, они стали выполняться реже, поскольку новые методы более точны и точны. Этими новыми технологиями являются сравнительная геномная гибридизация (CGH) и секвенирование следующего поколения (NGS).
Сравнительная геномная гибридизация (CGH)
Описание
Клетка человека содержит 23 пары хромосом. Анализ FISH позволяет точно оценить только 7-9 хромосом в каждой биопсийной клетке. Следовательно, многие аномальные эмбрионы, неспособные к формированию благополучной беременности, остаются незамеченными и могут быть перенесены.
Используя CGH, ядро эмбриона помечают флуоресцентным красителем, а контрольную клетку помечают другим цветом (например, красным или зеленым). Затем две клетки когибридизуют на контрольном метафазном спреде и сравнивают соотношение между двумя цветами. Если хромосомный анализ показывает избыток красного цвета, ядро эмбриона содержит лишнюю хромосому. Если наблюдается избыток зеленого, то в ядре эмбриона отсутствует одна из этих хромосом. CGH позволяет не только перечислить все 23 хромосомы, но и дает более подробную картину всей длины хромосомы, что может выявить дисбаланс хромосомных сегментов.
Источник: Progen
В настоящее время этот метод занимает 72 часа, и, учитывая ограниченную продолжительность жизнеспособности эмбрионов в культуре, для обеспечения времени, необходимого для постановки диагноза, требуется криоконсервация эмбрионов.
Исследования показали, что протоколы CGH не требуют криоконсервации и совместимы с переносом эмбрионов на 4–5-й день после оплодотворения. Это достигается либо с помощью массива CGH, ускоренного протокола CGH, дающего результаты за 24 часа для всех хромосом, либо с помощью биопсии полярного тела. В настоящее время немногие лаборатории предлагают эту технологию.
Секвенирование следующего поколения (NGS)
Описание
Новейшая технология, доступная для выполнения ПГТ, известна как секвенирование следующего поколения. В этом методе используется капиллярный электрофорез. Фрагментированные нити ДНК идентифицируют с использованием излучаемых сигналов и лигируют с матричной нитью. Методы амплификации, такие как ПЦР, используются для амплификации библиотеки ДНК. Затем выполняется секвенирование с использованием нескольких различных методов, включая секвенирование генома, экзома и секвенирование панели целевых генов. Из них секвенирование генома является самым дорогим, при этом он имеет самую низкую точность. При использовании секвенирования целевых генных панелей точность намного выше, а процесс намного быстрее и экономически эффективнее.
Источник: Progen
NGS позволяет проводить сравнительно быстрое секвенирование целых геномов, а также чрезвычайно подробное секвенирование целевых областей. Это позволяет использовать его в ПГТ-А, ПГТ-М и ПГТ-СП.
Хотя эти неинвазивные методы являются новыми и усовершенствовались за последние несколько лет, необходимо провести дополнительные разработки и исследования, чтобы обеспечить получение точных и согласующихся результатов с традиционными методами биопсии. Эти методы привлекательны для тех, кто проходит ПГТ, поскольку позволяет избежать большого количества манипуляций, которые необходимо выполнять с помощью традиционных методов ПГТ.
Можно ли проводить ПГД на замороженных эмбрионах?
Да, ПГД проводят на замороженных эмбрионах. Для этого эмбрионы должны быть извлечены из криоконсервации и успешно разморожены. В размороженных эмбрионах должно быть достаточно клеток, чтобы у врача была возможность отбора.
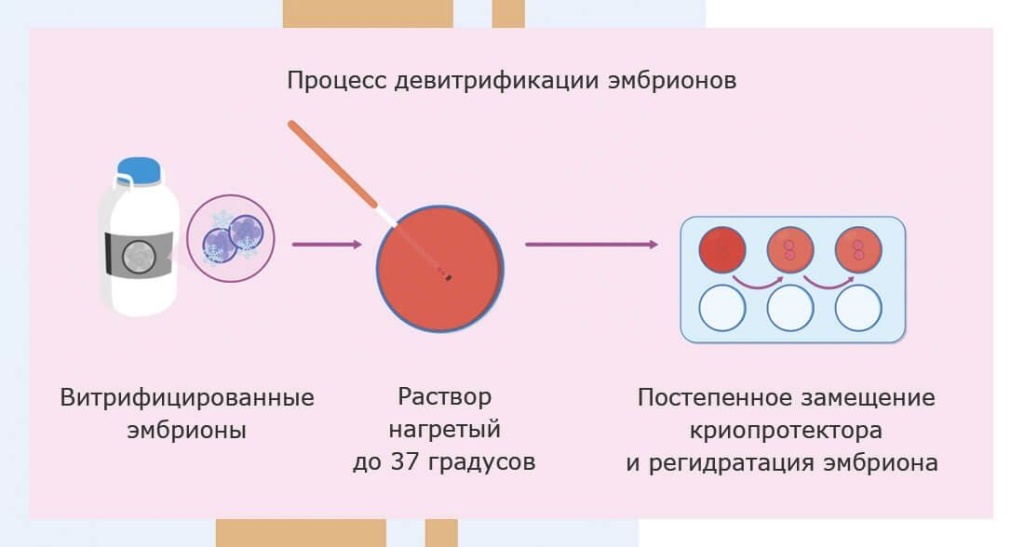
Процесс разморозки эмбрионов
Источник: Альтравита
Сколько стоит ПГД одного эмбриона?
Стоимость исследования ПГТ (ПГД) одного эмбриона зависит от того, на какие именно генетические аномалии вы проводите анализ, а также какие дополнительные исследования проводятся в дополнение к основному.
Так, анализ ПГТ-А одного эмбриона на анеуплодии в нашей лаборатории стоит 25 000 рублей. Анализ ПГТ-А анеуплоидий и триплоидии — уже 49 300 рублей. Понять, какой именно тест вам нужен, вы сможете на консультации с врачом-генетиком в нашем центре.
Узнать цены на все виды ПГТ (ПГД) вы можете в соответствующем разделе на нашем сайте
Сколько делается анализ ПГД?
В зависимости от типа анализа, ПГТ (ПГД) в нашей лаборатории проводится в срок от 14 до 30 рабочих дней. Так как это очень тонкий процесс с технической и научной точки зрения, мы стараемся не торопиться с ним в ущерб точности анализа. При этом мы гарантированно выполним тест в срок, указанный в карточке исследования на сайте.
Насколько достоверен анализ ПГД?
В большинстве случаев генетическое исследование выделенной ДНК в ПГТ результативно. А поскольку клетки трофэктодермы, которые берутся для анализа, и клетки внутриклеточной массы, дающие начало клеткам эмбриона, развиваются из одной оплодотворенной яйцеклетки, по результатам ПГТ лаборатория может однозначно дать заключение о том, поражен плод или нет. Исключение составляют мозаичные эмбрионы, когда в биоптате могут одновременно обнаруживаться клоны клеток с нормальным хромосомным набором и аномальные клетки. Хромосомный мозаицизм, по данным разных исследователей, описывается в 10–20% случаев. Для решения вопроса о переносе такого эмбриона требуется консультация врача-генетика.
Также необходимо помнить, что проведение ПГТ, даже когда оно результативно и не выявляет аномалий, не дает 100% гарантии здоровья будущего ребенка, поэтому семье, воспользовавшейся этим видом диагностики, необходимо в дальнейшем при наступлении беременности и рождении ребенка обязательно проходить рекомендованные врачом скрининговые исследования плода и новорожденного.